孕育养娃神器
无储存必要:胎盘/脐带间充质干细胞缘何不牵扯配型问题
提到移植,无论是器官移植,还是细胞移植,“配型”一直是备受关注的字眼。人们常说,配型犹如大海捞针,异常困难,以骨髓造血干细胞移植为例,配型成功率几万至几十万分之一的说法不等。而如今,医学界提出胎盘、脐带间充质干细胞不牵扯配型问题无储存必要的说法,这所谓的“配型”,究竟指的是什么?
一、什么是配型
配型,又称组织配型,核心为HLA分型匹配。HLA是Human Leukocyte Antigen的简拼,即“人类白细胞抗原”,广泛分布于机体内几乎所有有核细胞的表面。每个人的HLA千差万别,因此,HLA又有人体生物学的“身份证”之称。它是不同个体免疫细胞相互识别的标志,机体“区分敌我、识别自身、排除异已”的主要遗传标记,参与免疫应答反应,具有非常重要的生物学功能。因此在进行细胞移植时,供受者之间的HLA匹配程度反映了供受双方的组织相容性程度,和移植手术后的排斥反应率密切相关,决定了移植成功或失败,故又将其称为移植抗原。
HLA是一大类抗原分子的统称,虽然种类繁多,但免疫原性强弱不等,其中,以HLA-A、HLA-B、HLA-DRB1的免疫原性最强,与移植排斥反应关系最为密切,因此在干细胞移植配型时,首先对这三种抗原进行基因型匹配。而编码这三个抗原的基因位于两条同源染色体上,一条来自父方,一条来自母方,因此,共3×2=6个位点。这也就产生了我们常听到的“全相合、4个位点相合、5个位点相合”这样的说法。国内外大量的临床研究结果表明,受者和供者之间HLA相容程度越高,也就是受者和供者之间HLA-A、B、DR六个位点相合匹配的越多,排斥反应的发生率就越低,移植成功率就越高。反之,就越容易发生排斥反应,对患者术后的生存产生致命的危害。
二、配型为什么困难
对于干细胞移植,简单来说就是要将供者健康的、正常的干细胞移植到病人体内,来替换病人因疾病丧失功能的病态的、异常的细胞。比如公众广知的脐带血造血干细胞移植,或骨髓造血干细胞移植,就是先通过手术或放化疗的处理将体内原有的病态细胞杀死,再将供者的健康细胞移植入患者体内,这个过程中,由于受者本身的免疫系统通常极为脆弱,一旦发生排斥反应极易造成严重后果,引发患者死亡。因此,在移植上,通常要求6个位点至少有4个相合。
对于亲属来说,患者必然从父亲和母亲中各获得一条染色体,因而与父母的HLA为半相合(6个位点中3个匹配)。而对于兄弟姐妹,根据排列组合有4种情况,与患者有HLA完全一致的可能性为1/4,因此在进行移植时,通常首选在同胞兄妹中找寻供者(见图示)。
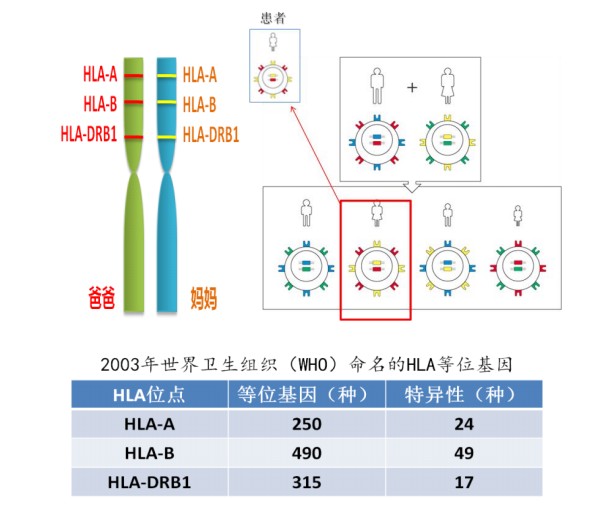
而对于无关供者来说,每一种抗原相应的等位基因有上百种,对应的特异性产物各自有数十种,如此复杂的基因及产物,可随机组合成一个巨大的数字,因此在随机人群中,难以有完全相同的HLA。这也就造就了我们说的“配型成功异常不易”。此外HLA的基因分布还有一定的民族、地域特点,所以,临床上很少见到白种人或黑种人与黄种人配型成功,这也使得跨国移植的情况显得非常稀缺。
正是这些等位基因的繁杂种类、位点相合的严格要求,使得干细胞移植的配型困难无比。
三、胎盘脐带间充质干细胞为什么无储存必要
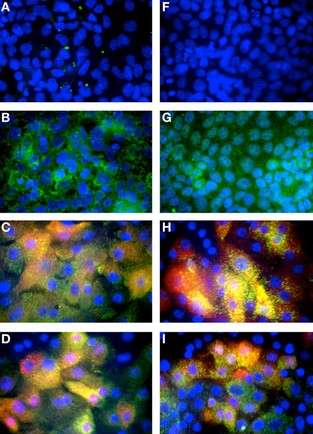
胎盘、脐带间充质干细胞,主要指从新生儿胎盘或脐带组织中提取的一种叫做间充质干细胞(Mesenchymal Stem Cell,MSC)的细胞。这类细胞的 HLA 抗原分子表达比较特殊,II 类分子不表达(如 HLA-DRB1),I 类分子低表达,此外还有其它一些免疫相关分子不表达或低表达,这使得间充质干细胞可以逃避机体免疫系统的识别,避开宿主监视,因而输注到体内不会引发很强的排斥反应。因此,在临床使用时无(无自体、异体区分)不牵扯HLA配型问题,加之其较易于分离、培养和扩增,无付费保存必要。
需要提醒的是,干细胞(造血干细胞、脐带血造血干细胞除外)治疗技术、自体免疫细胞治疗技术等作为未列入限制临床应用的医疗技术,现阶段无法应用于临床。也就是说,胎盘、脐带间充质干细胞无储存之必要。
 举报
举报
更多>>
更多>>